糖尿病,特别是Ⅱ型糖尿病,作为一组以高血糖为特征的代谢性疾病,已经成为严重的公共卫生问题。阻断和抑制人肠道中消化碳水化合物的酶,如α-淀粉酶,从而控制餐后血糖是一种有效缓解和治疗Ⅱ型糖尿病的方式。大量的研究是从天然产物中筛选众多的α-淀粉酶抑制剂并评价抑制活性,但是,常规的抑制活性筛选和评价方法,要么由于抑制剂的还原性干扰导致测试结果出现偏差,要么使用人造底物,从而都不能客观的反映α-淀粉酶消化天然淀粉的全貌。
我院岳田利教授团队开发出一种基于亲水色谱(HILIC)和质谱(MS)联用的方法用于评价α-淀粉酶的活性,并用于黄酮类化合物对α-淀粉酶抑制作用的评价。研究结果发表在国际食品TOP期刊Food Chemistry(Q1,IF:9.231)上,题为“Starch-digesting product analysis based on the hydrophilic interaction liquid chromatography coupled mass spectrometry method to evaluate the inhibition of flavonoids on pancreatic α-amylase” 。该研究得到国家博士后面上项目的支持,论文第一来源:yl6809永利为我院营养健康食品与安全控制团队肖郑操博士后,通讯来源:yl6809永利为岳田利教授,宋微副教授,论文第一单位为永利集团。
通过对色谱方法和质谱方法的优化,开发了基于HILIC-MS的α-淀粉酶活性评价系统。总共有11个酶促反应产物被识别,分别是聚合度2~12的葡聚糖寡糖。进一步的定量分析发现,聚合度为9的葡聚糖寡糖是酶促反应前期的主要产物,随着反应时间的增加,酶促反应产物逐渐以聚合度2,3,6和7的葡聚糖寡糖为主,这种α-淀粉酶产物的组成随时间变化的报道尚属首次。进一步基于该方法分析黄酮对于α-淀粉酶的抑可以发现,不同黄酮类化合物对于淀粉酶产物的抑制效果不尽相同,例如槲皮素主要抑制聚合度为2的麦芽糖的产生,而木犀草素则主要抑制聚合度更高的产物,这表明黄酮化合物结构差异影响了α-淀粉酶切割淀粉链的模式。本研究提供了一种全新的研究视角用于探索各种抑制剂对于α-淀粉酶的抑制作用,有助于研究者更好的评价抑制剂对于各种酶促产物的影响并解析抑制作用的机制。

研究亮点
用HILIC-MS方法表征了α-淀粉酶对淀粉的消化过程;
通过HILIC-MS评估了六种黄酮类化合物对α-淀粉酶的抑制特性;
黄酮醇和黄酮的3’位羟基增强了分子对于淀粉酶的抑制作用;
类黄酮的3位羟基降低了分子对淀粉酶高聚合度的产物的抑制作用。
研究结论
α-淀粉酶产物是1→4键连接的葡聚糖寡糖,聚合度介于2和12之间。聚合度为9的产物的产量最高,且在淀粉消化过程中先增加后减少。其他四种产物分别为2,3,6和7的产物产率在酶反应过程中不断增加。聚合度为4,5,8和10的产物产量相对较低。
花青素类化合物表现出比其他黄酮类化合物更好的抑制活性。
B环的3'-OH增强了黄酮醇和黄酮的抑制活性,但会降低花青素的抑制活性。
相比于黄酮,具有C环上3位羟基的黄酮醇对α淀粉酶低聚合度的产物有更好的抑制作用,但对较高聚合度酶促产物的抑制活性较弱。
图文赏析
·
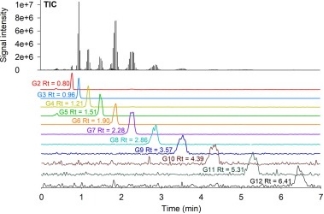
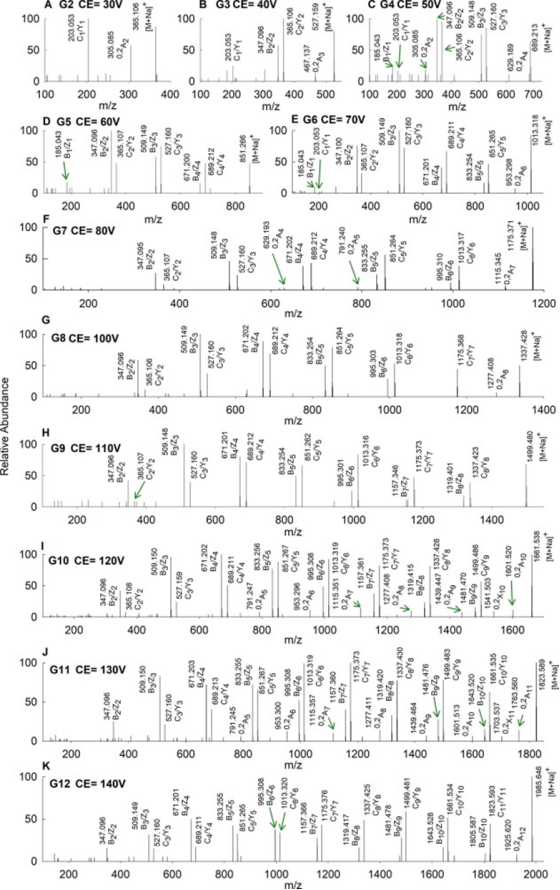
图1. α-淀粉酶产物的定性分析
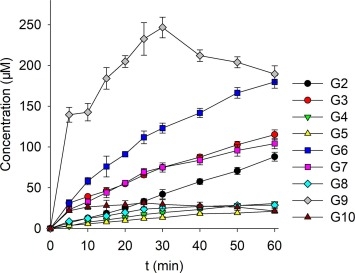
图2. α-淀粉酶产物的定量分析
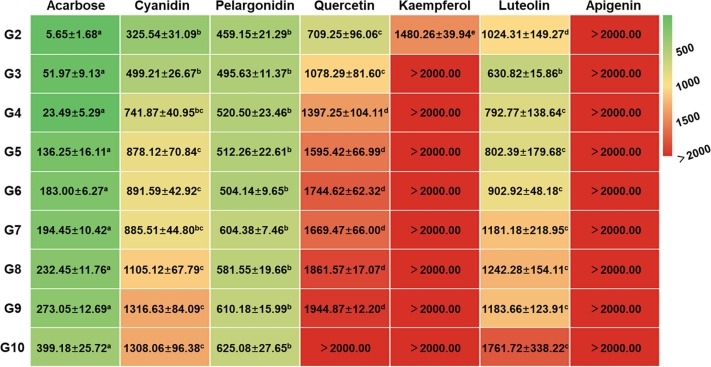
图3. 不同化学结构的黄酮类化合物对于α-淀粉酶产物的抑制作用